Sáng nay 15-8, tiêm thử nghiệm vaccine ARCT-154 công nghệ Mỹ sản xuất ở Việt Nam
Sáng nay 15-8, Trường Đại học Y Hà Nội đã khởi động chương trình thử nghiệm lâm sàng vaccine ARCT-154 ngừa Covid-19 giai đoạn 1 với sự tham gia của 100 tình nguyện viên ở Hà Nội.
Tại chương trình, Thứ trưởng Bộ Y tế Trần Văn Thuấn cho biết, ARCT-154 là vaccine được sản xuất theo công nghệ mRNA (tương tự Pfizer và Moderna) đầu tiên của Việt Nam, cũng là công nghệ tân tiến nhất hiện nay - saRNA (self-amplifying mRNA – mRNA tự nhân bản). Vaccine do Công ty CP Công nghệ sinh học VinBioCare thuộc Tập đoàn VinGroup đàm phán nhận chuyển giao công nghệ từ Công ty Arcturus Therapeutics, Inc, Hoa Kỳ.
Đáng chú ý, công nghệ mRNA cho phép sử dụng liều vaccine thấp hơn, trong khi kích thích miễn dịch kéo dài hơn, cho hiệu quả phòng ngừa biến thể SARS-CoV-2 nhanh chóng và đơn giản, có khả năng chống lại các biến chủng mới nguy hiểm như Alpha, Beta, Delta, Gamma. Hiện nay, các loại vaccine ngừa Covid-19 dựa trên công nghệ mRNA của Công ty Arcturus đã và đang được thử nghiệm lâm sàng giai đoạn 1, 2 và 3 tại Mỹ, Singapore và nhiều nước khác trên thế giới. Kết quả nhận được rất khả quan, tỷ lệ chuyển đổi huyết thanh đạt yêu cầu và đáp ứng độ an toàn, khả năng dung nạp. Đặc biệt, ARCT - 154 là vaccine có khả năng chống được biến chủng Delta đã được thử nghiệm giai đoạn 1,2 tại Singapore.
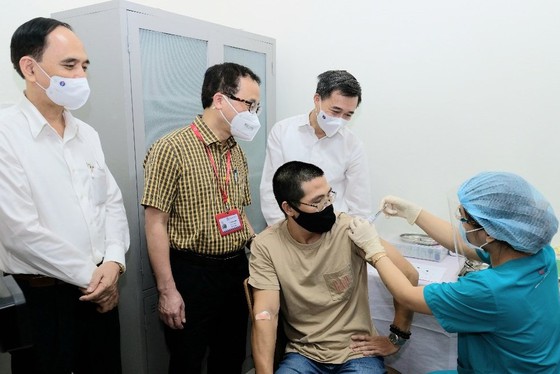 |
| Thứ trưởng Bộ Y tế Trần Văn Thuấn và đại diện Trường Đại học Y Hà Nội chứng kiến tình nguyện viên đầu tiên được tiêm thử nghiêm lâm sàng vaccine ARCT-154 |
Đối với Việt Nam, nghiên cứu phát triển vaccine ARCT-154 sẽ được thực hiện cả 3 giai đoạn 1, 2, 3 trên người tình nguyện tham gia nghiên cứu tuổi từ 18 tuổi trở lên.
Theo đó, giai đoạn 1: Khởi động vào ngày 15 và 16-8 với việc tiến hành tiêm mũi 1 cho 100 người tình nguyện khỏe mạnh tại Trung tâm thử nghiệm lâm sàng, Trường Đại học Y Hà Nội; giai đoạn 2: Thực hiện trên 300 người tình nguyện tại các tổ chức nhận thử và tại cộng đồng ở các tỉnh triển khai nghiên cứu; giai đoạn 3: Số lượng 20.600 đối tượng, gồm giai đoạn 3a (600 người tình nguyện) và 3b (20.000 người tình nguyện).
Thứ trưởng Trần Văn Thuấn cho biết thêm, đây là vaccine ngừa Covid-19 thứ 3 ở Việt Nam được cấp phép thử nghiệm lâm sàng trên người. Trước đó, vaccine Nano Covax (đang tiêm mũi 2 cho người tình nguyện ở giai đoạn 3b) và vaccine Covivac (đang tiêm mũi 1 giai đoạn 2).
GS Tạ Thành Văn, nghiên cứu viên chính, đại diện Đại học Y Hà Nội cho biết, quy trình tiêm thử nghiệm lâm sàng vaccine được thực hiện theo đúng đề cương do Bộ Y tế phê duyệt ngày 2-8.
Trong giai đoạn 1 có 100 người khoẻ mạnh đầu tiên tham gia tiêm thử nghiệm lâm sàng giai đoạn 1 được phân nhóm ngẫu nhiên theo tỉ lệ 3:1 (75% tiêm ARCT-154 và 25% tiêm giả dược). trước khi tiêm thử nghiệm, các tình nguyện viên được khám sàng lọc và làm các xét nghiệm.
Trong sáng nay đã có 25 tình nguyện viên được tiêm thử nghiệm vaccine ARCT-154. Mục tiêu chính của giai đoạn này là đánh giá tính an toàn và tính sinh miễn dịch. Người tình nguyện sẽ được tiêm 2 mũi vaccine ARCT-154 hoặc giả dược cách nhau 28 ngày. Các dữ liệu an toàn sau tiêm mũi 1 (ngày 1) đến 7 ngày sau tiêm mũi 2 (ngày 36) sẽ được đánh giá. Nếu dữ liệu này được Hội đồng Đạo đức Bộ Y tế đánh giá vaccine ARCT-154 thể hiện tính an toàn, khả năng dung nạp tốt, sẽ xin phép cơ quan quản lý tiến hành sớm thử nghiệm lâm sàng giai đoạn 2.
| Trước đó, thực hiện chỉ đạo của Thủ tướng Chính phủ và lãnh đạo Bộ Y tế về việc chuyển giao công nghệ vaccine Covid-19 để sớm có sản phẩm phục vụ công tác phòng chống dịch, Công ty CP công nghệ Sinh học VinBioCare đã đàm phán thành công với Công ty Arcturus Therapeutics, Inc, Hoa Kỳ. Theo đó, VinBioCare đã mua công nghệ vaccine mRNA phòng Covid-19 của Công ty Arcturus và triển khai đầu tư xây dựng nhà máy sản xuất vaccine tại Khu Công nghệ cao Hòa Lạc với tên gọi ARCT-154. |
(Theo sggp.org.vn)
 về đầu trang
về đầu trang