"Vũ khí mới" chống lại Covid-19
Cơ quan Quản lý dược phẩm châu Âu (EMA) ngày 6-10 thông báo đang cân nhắc triển khai quy trình đánh giá nhanh về Molnupiravir, loại thuốc điều trị Covid-19 dạng viên uống do hãng Merck & Co của Mỹ bào chế. Nếu được phê duyệt, đây sẽ là “vũ khí mới” chống lại Covid-19 trong thời gian tới.
 |
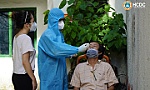
| Thuốc kháng virus dạng viên mở ra cơ hội cho việc điều trị Covid-19 |
Giảm triệu chứng, hạn chế lây nhiễm
Phát biểu với báo giới, ông Marco Cavaleri, phụ trách chiến lược vaccine tại EMA, cho biết, ủy ban cố vấn của cơ quan này có thể bắt đầu triển khai quy trình đánh giá nhanh dữ liệu về thuốc trong vài ngày tới. Trước đó, Merck & Co tuyên bố sẽ thúc đẩy Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) cấp phép sử dụng khẩn cấp thuốc Molnupiravir sớm nhất có thể, đồng thời thông báo hoàn thành sớm giai đoạn thử nghiệm do những kết quả tích cực mà loại thuốc này đem lại.
Theo Merck & Co, Molnupiravir (đang được thử nghiệm lâm sàng ở Seattle, bang Washington, Mỹ) có thể hỗ trợ giảm khoảng 50% nguy cơ nhập viện và tử vong đối với những trường hợp mắc Covid-19 có triệu chứng từ nhẹ đến trung bình. Merck & Co đang lên kế hoạch đăng ký tiếp thị Molnupiravir với các cơ quan quản lý dược phẩm trên thế giới.
Molnupiravir được nghiên cứu dựa trên thuốc gốc chống lại virus cúm, có tác dụng ức chế sự sao chép của các virus RNA, trong đó có SARS-CoV-2, khiến virus không nhân lên và bị đào thải rất nhanh, giúp bệnh nhân khỏi bệnh. Đặc biệt, thuốc có rất ít tác dụng phụ. Tuy nhiên, giới khoa học khuyến cáo, Molnupiravir cần được đánh giá và thử nghiệm trên một nhóm bệnh nhân lớn hơn nhiều để xác định chính xác mức độ an toàn.
Các nghiên cứu gần đây cho thấy, thuốc uống kháng virus có khả năng giảm bớt các triệu chứng và hạn chế lây nhiễm cho người xung quanh bệnh nhân. Ngoài Molnupiravir còn 2 ứng viên kháng virus khác là PF-07321332 do Pfizer nghiên cứu và AT-527 do Roche (Thụy Sĩ) và Atea Pharmaceuticals nghiên cứu. Pfizer đang thử nghiệm kết hợp giai đoạn 2 và 3 vào ngày 1-9. Còn Atea kỳ vọng có kết quả thử nghiệm giai đoạn 2 và 3 vào cuối năm nay.
Nếu cả 3 ứng viên đều đạt điều kiện, việc hàng triệu người được tiếp cận sớm với thuốc kháng virus có thể uống hàng ngày là chuyện khả thi. Đây là các loại thuốc dùng điều trị giai đoạn đầu của bệnh. Liệu trình thử nghiệm hiện tại là 1-2 liều mỗi ngày và sử dụng trong 5-10 ngày.
Các nước thu nhập thấp có cơ hội tiếp cận
Đầu năm nay, Merck & Co cũng tuyên bố đã ký thỏa thuận tự nguyện chuyển giao cấp phép cho 5 nhà sản xuất thuốc gốc tại Ấn Độ. Mục đích chính là giúp mở rộng khả năng tiếp cận thuốc điều trị ở hơn 100 quốc gia thu nhập trung bình và thu nhập thấp sau khi Molnupiravir được phê duyệt cấp phép khẩn cấp tại các nước.
Ngoài ra, Merck & Co dự kiến sẽ triển khai chiến lược giá bán nhiều mức ở từng nước, dựa trên tiêu chí thu nhập trung bình mà Ngân hàng Thế giới (WB) đưa ra. Merck & Co cho biết có thể sản xuất 10 triệu viên vào cuối tháng này. Ngoài Mỹ, Australia, Hàn Quốc, Malaysia, Thái Lan, lãnh thổ Đài Loan, đặc khu hành chính Hồng Công đã lên kế hoạch đặt hàng loại thuốc này.
Trong tháng này, WHO đã khuyến nghị sử dụng thuốc trị viêm khớp Actemra của Roche (Thụy Sĩ) và thuốc Kevzara của Sanofi (Pháp) cho bệnh nhân Covid-19 thể nặng. AstraZeneca vừa đệ trình hồ sơ đề nghị Mỹ cấp phép sử dụng khẩn cấp một loại thuốc kháng thể điều trị Covid-19 có tên gọi AZD7442. Đây là dạng thuốc tiêm hỗ trợ những người bị suy giảm miễn dịch, không phát triển phản ứng miễn dịch sau khi tiêm vaccine, tăng cường hệ miễn dịch đối với những người đã tiêm vaccine.
Loại thuốc kháng virus đang được nhiều quốc gia chấp thuận sử dụng điều trị Covid-19 là Remdesivir nhưng thuốc này được tiêm vào tĩnh mạch cho những bệnh nhân mắc bệnh đến mức phải nhập viện, không được dùng trong điều trị sớm và rộng rãi. Favipiravir cũng là loại thuốc có cơ chế tương tự như Remdesivir. Từ năm 2020, Trung Quốc là nước đầu tiên cấp phép sử dụng Favipiravir để điều trị Covid-19, sau đó các nước như Nga, Nhật Bản, Ấn Độ, Italy… cũng có quyết định tương tự.
(Theo sggp.org.vn)
 về đầu trang
về đầu trang